支持同片多轮顺序染色,在有限样本中整合更多靶标信息。
九色多重荧光染色试剂盒 Plus
基于 HRP-TSA 顺序染色原理的多重免疫荧光试剂盒,支持同一张切片的多轮多标检测,适用于 FFPE、冰冻组织、组织芯片及细胞样本,可用于多重免疫荧光、mIHC 与空间生物学研究中的 panel 搭建与成像流程开发。
适合弱表达与低丰度靶标的信号增强与可视化分析。
覆盖 FFPE、冰冻、TMA 及细胞样本的多重荧光工作流。
单张切片中完成多靶标检测,减少切片间偏差。
适合常规多通道采集,也适合高 plex 光谱拆分流程。
技术简介
九色多重荧光染色试剂盒 Plus 基于 HRP-TSA(Tyramide Signal Amplification)原理。HRP 催化活化后的 tyramide 荧光分子在靶标附近发生共价沉积,从而在保留已沉积荧光信号的同时,去除前一轮抗体复合物,支持同一张切片进行多轮顺序染色。该机制尤其适用于多标共表达研究、珍贵样本的多指标整合检测,以及需要兼顾低丰度与高丰度靶标的多重免疫荧光实验。
适合 mIHC / mIF 的多轮工作流
页面展示重点放在完整 TSA 解决方案,而不仅是荧光染料本身。该体系可以围绕样本前处理、panel 设计、顺序染色、成像采集和后续分析建立更稳定的多重荧光实验路径。
兼顾高信息密度与样本利用率
在有限组织面积、珍贵样本或需要保持空间结构上下文的实验中,可通过单片整合多靶标检测,提高信息产出并减少连续切片间的偏差。
核心优势
围绕高灵敏度、多轮顺序染色与高 plex 成像兼容性,构建更适合多重免疫荧光与空间生物学实验的技术路径。
高灵敏度信号放大
基于 HRP-TSA 的共价沉积机制,可增强弱表达和低丰度靶标的荧光可见度,适合需要提升检测灵敏度的多重免疫荧光实验。
支持同片多轮顺序染色
每轮检测完成后保留已沉积信号,并去除前一轮抗体复合物,便于在同一张切片上继续叠加下一个 marker。
降低同种属一抗交叉限制
由于沉积信号保留、抗体复合物可去除,panel 设计时更容易使用同种属一抗进行顺序组合,提高设计灵活度。
兼容空间生物学与高 plex 成像流程
适合与多光谱成像、spectral unmixing 及后续空间分析配合使用,用于降低荧光串扰并分离组织自发荧光背景。
适用样本类型
同类 TSA/mIF 公开工作流已用于 FFPE、细胞、组织芯片和冰冻切片,并可手工或自动化实施。这里作为同类 TSA/mIF 工作流的公开参考口径。
FFPE 石蜡组织切片
适合肿瘤组织、病理样本及需要保留组织结构信息的多标分析场景。
冰冻组织切片
可用于对部分抗原更友好的实验设计,适合与特定组织前处理流程配合优化。
组织芯片(TMA)
适合进行批量样本的一致化比较和 marker 空间表达差异评估。
细胞爬片 / 贴壁细胞样本
可用于细胞模型中的多标共表达验证、表型分析和细胞状态比较。
应用场景
面向多标共表达、空间关系与低丰度靶标检测等研究需求,帮助在同一组织上下文中获得更完整的信息。
肿瘤免疫微环境分析
在同一张切片中整合肿瘤细胞、T 细胞、巨噬细胞及免疫检查点标志物检测,支持表型分层与空间分布分析。
多标共表达与空间关系研究
在保留组织形态和空间上下文的前提下,同时观察多个 marker 的共表达、邻近关系与区域差异。
珍贵样本的多指标整合检测
适合样本量有限、切片珍贵或希望减少连续切片偏差的实验设计,在单片上获取更高信息密度。
低丰度靶标检测
针对荧光信号较弱、背景较高或表达水平较低的靶标,提供更适合的信号增强路径。
成像与光谱建议
本试剂盒适用于多通道荧光成像。对于低到中等 plex 的实验,可结合合适滤光片进行常规采集;对于高 plex、多色发射重叠明显或组织自发荧光较高的样本,更建议结合多光谱成像与 spectral unmixing,以降低 fluorophore crosstalk,并将组织自发荧光分离为独立背景通道,从而提高定量可靠性。
试剂盒组成
试剂盒提供 TSA 反应所需的核心荧光底物、缓冲体系、HRP 通用二抗、DAPI、抗体稀释液、过氧化氢封闭液及抗淬灭封片剂,适用于多轮顺序染色工作流。具体颜色组合与适配 panel 请以最终确认版产品技术手册为准。
| 模块 | 内容 | 说明 |
|---|---|---|
| 荧光底物体系 | 多重 TSA 荧光底物 | 用于多轮顺序染色中的信号沉积与多标检测。 |
| 检测体系 | HRP 通用二抗 | 配合一抗和 TSA 反应完成靶标识别与信号放大。 |
| 染色辅剂 | 抗体稀释液、缓冲体系 | 用于抗体配置、反应稳定性与多轮染色流程衔接。 |
| 封闭与背景控制 | 过氧化氢封闭液 | 帮助降低内源性过氧化物酶带来的背景干扰。 |
| 复染与封片 | DAPI、抗淬灭封片剂 | 支持细胞核复染与成像前稳定封片。 |
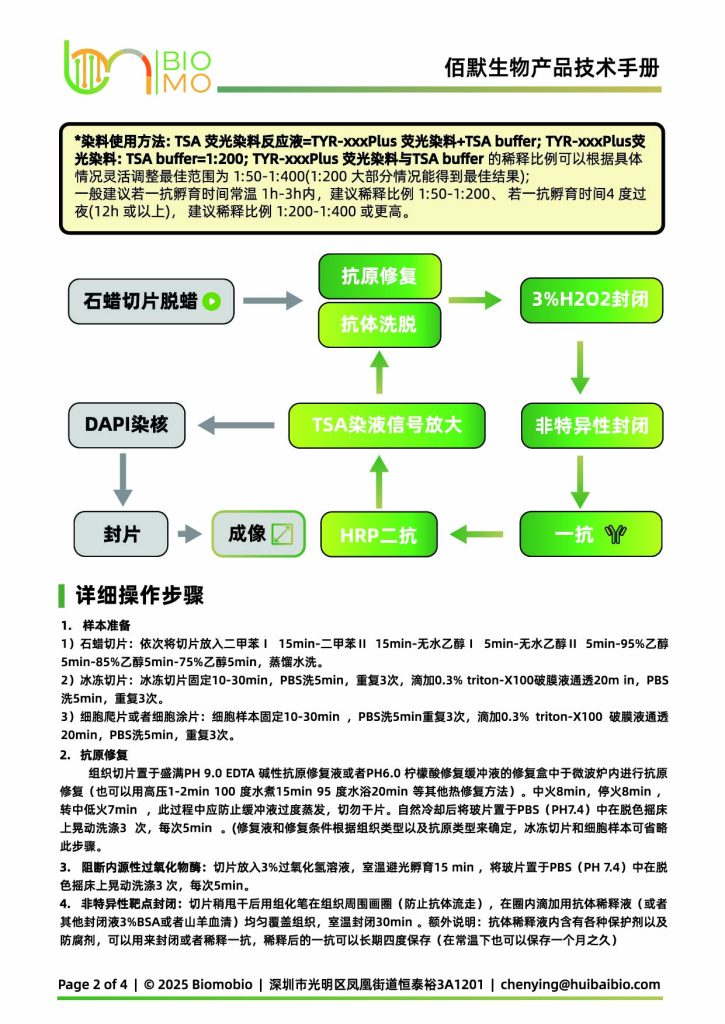
标准多重染色流程
核心原理:染色 → 荧光沉积 → 去除抗体 → 下一轮染色。该逻辑与公开 TSA/mIF 工作流一致,即利用结合在靶标上的 HRP 系统激活 tyramide,在靶标附近完成沉积,然后通过串行 stripping 进入下一轮标记。
样本前处理
石蜡切片脱蜡复水,或细胞样本固定与预处理。
抗原修复
根据抗原特性选择 EDTA 或柠檬酸体系,并统一控制修复条件。
封闭与一抗孵育
完成背景封闭后进行第一轮一抗孵育与条件优化。
HRP 通用二抗孵育
构建后续 TSA 反应所需的酶催化检测体系。
TSA 荧光底物反应
完成荧光信号沉积,保留本轮靶标的稳定标记。
去除前一轮抗体复合物
在保留沉积信号的前提下移除上一轮抗体体系,为后续 marker 腾出检测空间。
重复步骤 3–6
按照既定 panel 顺序继续完成下一轮靶标染色。
DAPI 复染与成像分析
完成核染、抗淬灭封片以及后续多通道或多光谱采集分析。
实验设计与质控建议
高 plex TSA/mIHC 实验更依赖前期验证和 panel 顺序设计。建议在进入正式多标实验前完成单标验证、背景评估与成像条件确认。
先做单标验证
每支一抗建议先完成单 marker 染色验证和稀释度优化,再纳入多标 panel。
配置必要对照
建议设置阳性、阴性、未染及必要的单染对照,用于评估背景、自发荧光和光谱拆分稳定性。
考虑顺序与染料分配
panel 设计需综合抗原丰度、信号强度、染料匹配关系和染色顺序,避免强弱信号失衡。
统一样本前处理
FFPE 样本建议标准化固定、切片保存和前处理流程,以提高批次间重现性与可比性。
数据分析与结果输出思路
多重免疫荧光实验的价值不仅在于染色本身,也在于后续图像拆分、细胞分型、空间关系量化和候选结果解释。
分析步骤
检查曝光、背景、自发荧光和通道间串扰情况。
在需要时结合 spectral unmixing 进行荧光分离与背景校正。
依据核和 marker 组合完成细胞识别与群体分类。
分析不同细胞群之间的距离、邻近关系和区域富集特征。
可交付图表类型
用于展示 marker 分布与整体组织结构关系。
展示不同细胞亚群的组成比例和空间定位。
用于评估细胞间相互作用和局部富集趋势。
支持不同区域或不同样本间的对比分析。
常见问题
围绕样本兼容性、panel 设计与高 plex 成像的常见问题,提前明确实验边界和优化重点。
可用于 FFPE、冰冻组织、组织芯片和细胞样本,具体前处理和 panel 优化建议根据样本类型单独确认。
TSA 体系的关键优势之一,就是已沉积信号保留、抗体复合物去除,因此更适合进行同种属一抗的顺序 panel 设计。
不是所有实验都必须,但当通道数增加、发射光谱接近或样本自发荧光较高时,多光谱采集结合 spectral unmixing 会更稳妥。
因为 TSA 放大会显著改变信号强度和背景平衡,多标 panel 需要单独优化一抗浓度、染料分配和染色顺序。
同类 TSA/mIF 工作流可用于手工或自动化实施。是否接入具体平台,需要结合仪器流程、抗原修复条件和 panel 设计进一步确认。
可以,但建议根据抗原丰度、信号强弱和染色顺序进行整体设计,使强信号与弱信号之间获得更均衡的成像结果。